Vielleicht denkst du jetzt „Gas? Im Aquarium? Ist Gas nicht immer irgendwie Luft?“
Der Gedanke ist nicht falsch, aber Gase können sich tatsächlich auch in Flüssigkeiten lösen!
Was ist also der Unterschied zwischen einem Gas und einer Flüssigkeit?
Alles auf der Welt besteht aus so genannten Atomen, das sind ganz winzig kleine Teilchen. Davon gibt es verschiedene Arten, so zu sagen „Grundstoffe“. Diese Grundstoffe können sich wie Bausteine zusammensetzen und wiederum andere Stoffe bilden. Ein aus mehreren Atomen zusammengesetztes Teilchen nennt man ein Molekül. Auf diese Art kommen alle Materialien der Welt zu Stande!
Ob etwas dann gasförmig, flüssig oder fest ist, kommt darauf an, wie diese Teilchen verbunden sind.
In Gasen sind sie gar nicht verbunden – die Atome fliegen einfach herum und versuchen einen größtmöglichen Abstand zu einander zu halten. Deshalb ist Luft so „dünn“ – du kannst darin nicht schwimmen, weil einfach zu wenig Teilchen darin unterwegs sind, an denen du dich abstützen könntest. Dass aber in Wirklichkeit etwas da ist, sieht man an Drachen, Vögeln und Flugzeugen: Sie sind darauf spezialisiert, auch in dem wenig dichten Gasgemisch „Luft“ noch ausreichend Widerstand für Bewegung zu finden.
In Flüssigkeiten können sich die Atome auch frei bewegen, aber sie gehen dort auf „Kuschelkurs“ und sind ganz dicht beieinander.
Schauen wir uns kurz die Flüssigkeit an, mit der wir es in der Aquaristik zu tun haben: Wasser. Ein einzelnes Wassermolekül ist aus zwei Atomen von Wasserstoff (Kurz „H“) und einem von Sauerstoff (kurz „O“) aufgebaut. Die Buchstaben gehen auf die lateinischen Bezeichnungen zurück, „Hydrogenium“ = Wasser, „Oxygenium“ = Sauerstoff. Das Molekül beschreibt man mit der Abkürzung „H2O“. („Von Wasserstoff 2, von Sauerstoff 1“.)
Eine Menge dieser Moleküle ergibt Wasser. Im Gegensatz zu Gas ist Wasser so dicht, dass wir darin schwimmen können. Wenn du einen Schwimmzug machst, stößt du dich tatsächlich an vielen Millionen Wassermolekülen ab! Die sind ein bisschen träge und gehen nicht sofort auseinander, deshalb funktioniert das.
Und Feststoffe? Ganz klar, hier sind die Moleküle dicht, fest miteinander verbunden und weichen gar nicht aus. Ein Stein, Holz, Metall – alles bei normalen Temperaturen Feststoffe.
Was passiert bei anderen Temperaturen? Das ist ein wichtiger Knackpunkt! Die Stoffe können je nach Temperatur ändern, ob sie fest, flüssig oder gasförmig sind. Man nennt diese Zustände übrigens „Aggregatzustände“ („Aggregat“ = Ansammlung).
Im Allgemeinen ist es so, dass die Stoffe im kalten Zustand fest, im mittleren flüssig und im warmen gasförmig sind. Wann der jeweilige Übergang stattfindet, ist aber von Stoff zu Stoff ganz unterschiedlich. Deshalb sind bei „normalen“ Temperaturen einige Stoffe fest, andere flüssig und manche gasförmig.
Am anschaulichsten sieht man diesen Wechsel beim Wasser: Kalt ist es festes Eis, mittelwarm flüssig und wenn man es zum kochen bringt, steigt das Wasser als Dampf gasförmig auf. Es „verschwindet“ dabei nicht, sondern die Wassermoleküle fliegen unsichtbar in der Luft herum.
Ein Thermometer nutzt den Zustandswechsel von Wasser als Skala nach Celsius: 0° ist der Schmelzpunkt, also Eis wird Wasser, und 100° ist der Siedepunkt, also Wasser wird zu Dampf.
wBei anderen Stoffen sind diese Punkte ganz woanders. Sauerstoff zum Beispiel wird bei unter minus 218° fest – also erst, wenn es furchtbar kalt ist. Bis minus 183° ist er flüssig. Solche Temperaturen gibt es auf der Erde nicht, das heißt, wir treffen Sauerstoff nur gasförmig an. Wie er trotzdem ins Wasser kommt, erklären wir gleich.
[box type=“info“ align=““ class=““ width=““]Die Atmosphäre der Erde, also die Luft, enthält Gase in folgendem Verhältnis:
78% Stickstoff
21% Sauerstoff
1% andere Gase, wie Argon, Kohlenstoffdioxid (0,04%) und Wasserdampf[/box]
Mit diesen wichtigen Hintergrundinfos im Kopf wenden wir uns jetzt unseren Aquarien zu. Zwei Gase spielen dort eine besonders wichtige Rolle: Sauerstoff (O2) und Kohlenstoffdioxid (CO2). Etwas vereinfacht dargestellt funktioniert das so: Die Tiere brauchen Sauerstoff zum Atmen, genauso wie die Bakterien, um Stoffwechselprodukte abzubauen. Dabei kommt Kohlenstoffdioxid, also CO2, heraus. Das brauchen wiederum die Pflanzen zum Wachsen. Es ist also eigentlich ein Kreislauf. Aber leider ist der nicht ganz ungestört – im Dunkeln produzieren Pflanzen keinen Sauerstoff, sondern verbrauchen selber welchen.
Es entsteht also ein ständiger Wechsel:
Tagsüber: Fische und Bakterien verbrauchen Sauerstoff und produzieren CO2. Die Pflanzen verarbeiten das CO2 und produzieren Sauerstoff. Das Wasser wird mit Sauerstoff gesättigt, der CO2 Gehalt sinkt.
Nachts: Alle Lebewesen verbrauchen Sauerstoff und produzieren CO2. Der Sauerstoffgehalt sinkt, das CO2 steigt.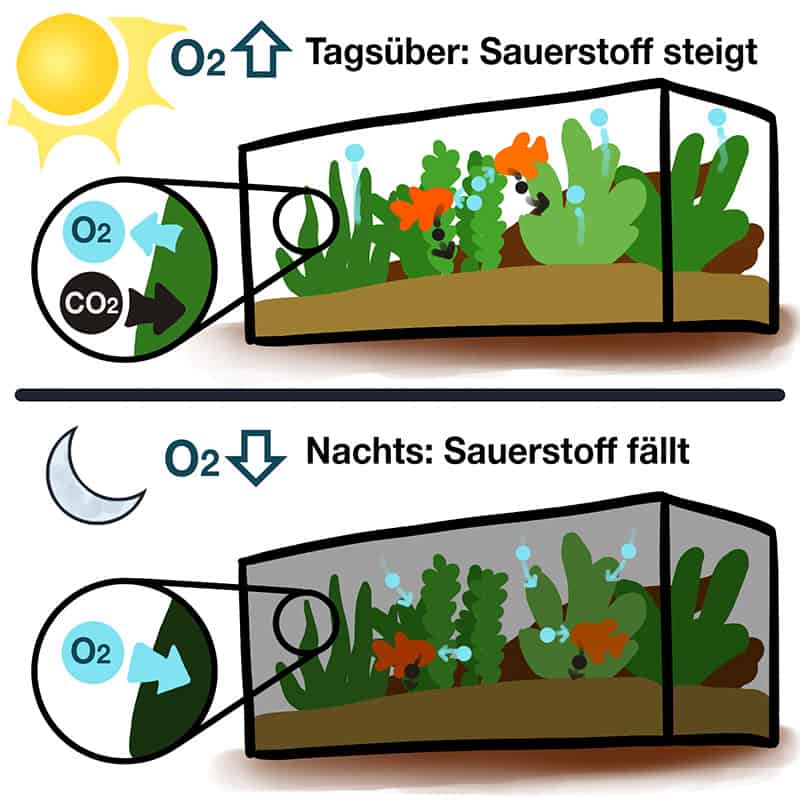
All das passiert recht gemächlich, und beschränkt sich nicht auf das Wasser. Das Wasser hat ja Kontakt zur Luft – an der ganzen Oberfläche findet ein steter Austausch statt. Sowohl Sauerstoff, als auch Kohlenstoffdioxid können von der Luft ins Wasser übergehen und umgekehrt – was davon sie tun, kommt auf die Umstände an. Das erklären wir im Folgenden.
Gase haben die Eigenschaft, sich möglichst gleichmäßig zu verteilen. Ist in Flüssigkeiten Platz für Gasmoleküle, „schlüpfen“ sie auch dort hinein und beschränken sich nicht nur auf die Luft. Wie viele der Gasmoleküle in eine Flüssigkeit – in unserem Fall Wasser – passen, wird durch die Flüssigkeit bestimmt.
Bei dem für uns besonders wichtigen Beispiel Wasser / Sauerstoff entscheidet darüber die Temperatur.
Kaltes Wasser bietet mehr freie Plätze für Sauerstoffmoleküle, wärmeres weniger.
Bei 0° C ist Platz für 14,6 Milligramm Sauerstoff in einem Liter Wasser.
Bei 10 °C sind es 11,3 mg/l,
bei 20° C 9,1 mg
bei 25° C noch 8,2 mg/l
bei 30° C nur noch 7,6 mg/l
Du siehst also, in 30° warmem Wasser ist nur noch etwa halb so viel Sauerstoff wie in 0° kaltem Wasser.
Zum einen produzieren die Pflanzen tagsüber beim Wachsen Sauerstoff, das nennt man Photosynthese. Und zum anderen kommt er einfach aus der Luft und drängt sich, wie bereits beschrieben, in die „freien Plätze“ im Wasser. Das können die Sauerstoffmoleküle natürlich nur von der Luft aus, also an der Wasseroberfläche. Nun sind Moleküle aber ganz winzig klein, und nicht besonders schnell. Das bedeutet, wenn unten im Wasser freie Plätze sind, brauchen sie ziemlich lange, um dorthin zu wandern und direkt unter der Oberfläche bildet sich sozusagen eine „Schlange“. Es können erst mehr Sauerstoffmoleküle nachrücken, wenn die Ersten weiter nach unten gewandert sind.
Wenn also über Nacht viel Sauerstoff verbraucht wird, fällt der Sauerstoffgehalt besonders im unteren Bereich des Beckens und der von der Oberfläche nachwandernde Sauerstoff kommt nicht so schnell dorthin, wie er verbraucht wird.
Durch zwei Dinge kann hier Abhilfe geschaffen werden: Erstens durch Umwälzung, also das Vermischen der Wasserschichten. Ist der Filterauslass so eingestellt, dass er die Oberfläche bewegt, wird das frisch mit Sauerstoff aufgeladene Wasser von dort in andere Bereiche des Aquariums bewegt und „leeres“ Wasser zum Aufladen an die Oberfläche befördert. So kann man den Austausch zwischen Luft und Wasser deutlich beschleunigen und den Gashaushalt ausgleichen.
Und zweitens durch eine Luftpumpe. Die unzähligen Blasen haben gemeinsam eine riesig große Oberfläche, der Sauerstoff wird praktisch ins Wasser gedrückt. Das ist also der „Express“ für den nachwandernden Sauerstoff.
Beim CO2 läuft es etwas anders. Der Gehalt von CO2 im Wasser ist nicht von der Temperatur abhängig, sondern von zwei Wasserwerten: Ph, also dem Säuregrad, und KH, der Karbonathärte. Diese drei Werte stehen in einem festen Verhältnis zueinander:
Je geringer die Karbonathärte, desto geringer der CO2 Gehalt.
Aber je höher der pH Wert, desto niedriger ist CO2.
Die Extreme sind also:
Man kann dieses Verhältnis in Tabellen wie dieser ablesen:
Um CO2 zu beeinflussen, kann man also pH oder KH ändern. Aber auch umgekehrt mit der Zugabe von CO2 über eine Düngung den pH Wert senken.
Die KH bleibt dabei fest. Nehmen wir an du hast eine KH von sechs und einen pH Wert von 7,5. Dann sind 6 mg CO2 pro Liter Wasser vorhanden. Das ist etwas wenig für die Pflanzen. Wenn du nun also CO2 zudüngst, steigt der Wert von CO2 im Wasser und zieht damit den pH Wert runter. Düngst du so viel, dass du 18 mg/l CO2 hast, fällt der pH Wert auf 7. Faszinierend, oder?
Ja! Wenn alle Plätze belegt sind, kommt kein Gas mehr herein. Ist das Wasser überbelegt, läuft das ganze andersrum. Gasmoleküle lösen sich aus dem Wasser heraus und fliegen davon in die Luft. Dabei hat jedes Gas seinen eigenen Sättigungsgrad. Wenn das Wasser also beispielsweise mit Sauerstoff komplett gesättigt ist, also bei 25° mehr als 8,2 mg/l im Wasser sind, kann CO2 immer noch unabhängig davon im Wasser Platz finden, aber Sauerstoff „gast aus“, löst sich also aus dem Wasser und ist wieder Gas in der Luft.
 Jain. Mit dem Sauerstoff hat das eigentlich nichts zu tun, die beiden Gase sind unabhängig voneinander. Allerdings hat der Betrieb einer Luftpumpe tatsächlich den Nebeneffekt, dass CO2 abtransportiert wird. Denn in Luft ist davon im Verhältnis viel weniger als im Wasser und nur die Trägheit des Systems sorgt dafür, dass zum Beispiel zugedüngtes CO2 im Wasser bleibt und nur langsam über die Oberfläche entweicht. Mit der Belüftung bietet man dem CO2 sozusagen einen Schnellzug nach draußen.
Jain. Mit dem Sauerstoff hat das eigentlich nichts zu tun, die beiden Gase sind unabhängig voneinander. Allerdings hat der Betrieb einer Luftpumpe tatsächlich den Nebeneffekt, dass CO2 abtransportiert wird. Denn in Luft ist davon im Verhältnis viel weniger als im Wasser und nur die Trägheit des Systems sorgt dafür, dass zum Beispiel zugedüngtes CO2 im Wasser bleibt und nur langsam über die Oberfläche entweicht. Mit der Belüftung bietet man dem CO2 sozusagen einen Schnellzug nach draußen.
Insofern macht es wenig Sinn, gleichzeitig CO2 zu düngen und zu belüften. Besser ist es hier, zu wechseln: Sauerstoffmangel herrscht meistens nachts und Pflanzen brauchen CO2 nur bei Licht. Also belüftet man bei Bedarf nachts und macht tagsüber die Pumpe aus und stattdessen CO2 an.

Und wenn du doch mal nicht weiter kommst mit deinem Aquarium, eine Frage oder Anregungen hast: Schreib‘ Mr. Fishy!

Wir haben Ende 2018 dieses neue Format gestartet und werden in Zukunft auf diesem Kanal alles abdecken, was dich als Aquarianer unterstützt und dir hilft, dein Aquarium besser und gesünder zu betreiben.

Was beschäftigt die Aquaristik-Community? Der my-fish-Newsletter informiert dich über spannende Inhalte aus der Unterwasserwelt.

Wir haben bei Zierfischgroßhändlern, Aquascapern, Züchtern und Liebhabern nachgefragt: